ミカファンギン(英語:Micafungin 略称:MCFG 商品名:ファンガード)の特徴と投与方法をまとめます。
- MCFGはβ-(1,3)-Dグルカン合成を阻害し、カンジダに殺菌的に、アスペルギルスに静菌的に作用する。β-(1,6)-Dグルカンが主体のムーコル、フサリウム、トリコスポロン、クリプトコックス、α-Dグルカンが主体の酵母相の二相性真菌に効果が乏しい。
- 予防の例 MCFG 50mg + 生食100mL 1日1回30分でdiv
治療の例 MCFG 100〜150mg + 生食100mL 1日1回1時間でdiv - CNSへの移行性は不良。主な副作用は肝障害。肝障害・腎障害での減量なし。
MCFGの位置付け
エキノキャンディン系の作用機序
アゾール、ポリエン、フルシトシンに次ぐ4番目の抗真菌薬として登場したのが、エキノキャンディン系です。
エキノキャンディン系は真菌細胞壁のβDグルカン合成を阻害します。βDグルカン合成酵素のサブユニットFks1pに非競合的に結合して、その酵素を阻害します。カンジダに対して殺菌的に、アスペルギルスに対して静菌的に作用します。Szymański M, Chmielewska S, Czyżewska U, Malinowska M, Tylicki A. Echinocandins – structure, mechanism of action and use in antifungal therapy. J Enzyme Inhib Med Chem. 2022;37: 876–894.
非競合的阻害剤で、濃度依存性があり、臨床ではMCFG 50〜300mgまで調節(※ CPFGは肝障害や相互作用以外で原則調節なし)されます。アゾールやポリエンとは作用機序が異なるため、相加・相乗効果を期待して併用療法も研究されています。Chandrasekar PH, Sobel JD. Micafungin: a new echinocandin. Clin Infect Dis. 2006;42: 1171–1178.
エキノキャンディン系が阻害するのはβDグルカンの中でも、β-(1,3)-Dグルカンです。したがって、主にβ-(1,6)-Dグルカンで真菌細胞壁を構成しているムーコル、フサリウム、トリコスポロン、クリプトコックス等には効果が乏しいです。また二相性真菌は糸状菌相ではβ-(1,3)-Dグルカンが豊富ですが、二相性真菌の酵母相はα-Dグルカンが豊富で効果が乏しいです。
エキノキャンディン系投与中の酵母様真菌のブレイクスルーでは、耐性カンジダに加えて、トリコスポロンが重要です。
エキノキャンディン系の種類
主なエキノキャンディン系は下記の4種類です。
- CPFG(カスポファンギン、商品名カンサイダス)
- MCFG(ミカファンギン、商品名ファンガード)
- ANFG(アニデュラファンギン) ※日本で未承認
- RZFG(レザファンギン) ※日本で未承認、週1回投与
日本では2002年にMCFGが、2012年にCPFGが認可されました。アメリカでは逆にCPFGのほうが先に認可されており、歴史的には先にCPFGが開発され、その後2番目のエキノキャンディン系としてMCFGが開発された流れです。
カンジダの専門家
MCFGは主にカンジダをカバーします。アゾール系より副作用・相互作用が少ないため、カンジダを中心にカバーしたい時に頻用されています。アスペルギルスに関してはVRCZが第一選択です。酵母と糸状菌の両形態をとる二相性真菌に関して、特に酵母相の時にMCFGは無効です。
MCFGはカンジダの専門家です。
| FLCZ | ITCZ VRCZ PSCZ ISCZ | MCFG CPFG | L-AMB | |
|---|---|---|---|---|
| カンジダ | ||||
| アスペルギルス | ||||
| 二相性真菌 |
MCFGのカンジダへのスペクトラムについて、詳しく見ていきます。
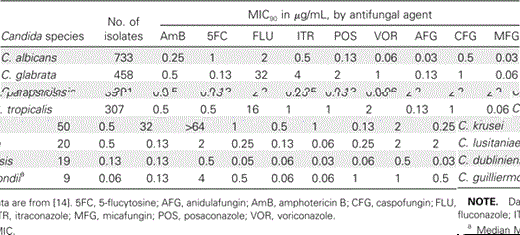
C. albicans、C. tropicalis、C. glabrata 等に対して、CPFGよりもMCFGのほうがin vitroでの阻害活性が5〜10倍増加するという報告があります。Ostrosky-Zeichner L, Rex JH, Pappas PG, Hamill RJ, Larsen RA, Horowitz HW, et al. Antifungal susceptibility survey of 2,000 bloodstream Candida isolates in the United States. Antimicrob Agents Chemother. 2003;47: 3149–3154.
C. parapsilosis へのMICがやや高めであり、臨床的意義は明確ではありませんが、注意します。Pfaller MA, Boyken L, Hollis RJ, Kroeger J, Messer SA, Tendolkar S, et al. In vitro susceptibility of invasive isolates of Candida spp. to anidulafungin, caspofungin, and micafungin: six years of global surveillance. J Clin Microbiol. 2008;46: 150–156.
C. glabrata では、FKS変異によるエキノキャンディン系耐性株に注意します。添付文書でも注意が促されています。
C. guilliermondii では、耐性菌が少し多く、下記の表では△と記載しました。
C. auris について、2018年のメタアナリシス及びシステマティック・レビューで耐性率は低いと報告されており、下記の表では◯と記載しました。Osei Sekyere J. Candida auris: A systematic review and meta-analysis of current updates on an emerging multidrug-resistant pathogen. Microbiologyopen. 2018;7: e00578.
しかしながら、FKS変異によるMCFG耐性の報告があり、注意します。Chow NA, Muñoz JF, Gade L, Berkow EL, Li X, Welsh RM, et al. Tracing the Evolutionary History and Global Expansion of Candida auris Using Population Genomic Analyses. MBio. 2020;11. doi:10.1128/mBio.03364-19
また、C. auris に対して、MCFG・CPFG・anidulafungin(ANFG)よりもrezafungin(RZFG)が優れる可能性も指摘されています。Kovács R, Tóth Z, Locke JB, Forgács L, Kardos G, Nagy F, et al. Comparison of In Vitro Killing Activity of Rezafungin, Anidulafungin, Caspofungin, and Micafungin against Four Candida auris Clades in RPMI-1640 in the Absence and Presence of Human Serum. Microorganisms. 2021;9. doi:10.3390/microorganisms9040863
| 出現頻度[%] | FLCZ | ITCZ | VRCZ | PSCZ | ISCZ | MCFG | CPFG | |
|---|---|---|---|---|---|---|---|---|
| C. albicans | 40-60 | |||||||
| C. parapsilosis | 5-30 | |||||||
| C. tropicalis | 5-30 | |||||||
| C. krusei | 2-4 | |||||||
| C. glabrata | 5-30 | |||||||
| C. lusitaniae | 0.5-1 | |||||||
| C. kefyr | 0.5-1 | |||||||
| C. guilliermondii | 0.5-1 | |||||||
| C. auris | <0.01 |
アスペルギルスに対しては、L-AMBが自然耐性のA. terreusを含めてカバーするものの静菌的です。
| FLCZ | ITCZ | VRCZ | PSCZ | ISCZ | MCFG | CPFG | L-AMB | |
|---|---|---|---|---|---|---|---|---|
| A. fumigatus | ||||||||
| A. flavus | ||||||||
| A. niger | ||||||||
| A. terreus |
MCFGは希少深在性真菌症にほとんど無効です。MCFGは頻用されていますが、真菌へのスペクトラムは狭い抗真菌薬である点に注意します。MCFG投与中のブレイクスルー真菌感染では、VRCZへのクラススイッチが合理的ですが、その場合ムーコルをカバーできず、一方でPSCZ・ISCZ・L-AMBへのクラススイッチではフサリウム等へのカバーが甘くなります。
| FLCZ | ITCZ | VRCZ | PSCZ | ISCZ | MCFG | CPFG | L-AMB | |
|---|---|---|---|---|---|---|---|---|
| ムーコル | ||||||||
| フサリウム | ||||||||
| トリコスポロン | ||||||||
| スケドスポリウム | ||||||||
| クリプトコックス |
移行性
MCFGは眼や中枢神経系への移行性が悪いです。眼内炎や真菌性髄膜炎に無効です。
中枢神経系への移行性
良好:FLCZ、VRCZ、ISCZ、L-AMB
不良:ITCZ、PSCZ、MCFG、CPFG
MCFGの投与方法
点滴
経口投与ではほとんど吸収されないため、剤型は点滴のみです。
25mg, 50mg, 75mgの3種類があります。
薬価は、25mgの先発品が約2000円、後発品が約1000円、50mgの先発品が約3000円、後発品が約1500円、75mgの先発品が約4500円、後発品が約2000〜2500円です。後発品は先発品のおおよそ半額となっています。現在では後発品を採用している病院が多いでしょうから、50mgで約1500円、150mgで約4500円かかると覚えておくと良さそうです。
CPFGはローディングが必要ですが、MCFGは不要です。
予防で MCFG 50mg + 生食100mL 1日1回30分でdiv
治療で MCFG 100〜150mg + 生食100mL 1日1回1時間でdiv
溶解液は5%ブドウ糖も可です。
速度に関して、75mg以下は30分以上、75mg以上は1時間以上の規定があります。半減期は11〜17時間で、1日1回投与で済みます。
投与量に関して、予防で1mg/kgを超えないこと、治療で6mg/kgを超えないことという規定がありますので、体重50kg以下では配慮します。
その他、配合直後に濁りが生じたり、力価が低下したりする薬剤があり、注意します。調製後〜点滴終了まで6時間以上かかる場合には遮光しておきます。TDMは不要です。
腎障害・肝障害
MCFGは腎障害・肝障害での用量調節は規定されていません。
対照的にCPFGは肝障害で用量調節があります(Child-Pugh Bで50→35mgへ)。
MCFGの副作用・相互作用
副作用
エキノキャンディン系がターゲットとするβDグルカンはヒトの細胞には存在せず、副作用は少ないです。
最も注意するのは肝障害ですが、VRCZより少なく、FLCZやL-AMBと同じくらいの頻度です。高Bil血症2.9〜13.3%、AST・ALT上昇0.7〜6.8%と報告されています。Chau MM, Daveson K, Alffenaar J-WC, Gwee A, Ho SA, Marriott DJE, et al. Consensus guidelines for optimising antifungal drug delivery and monitoring to avoid toxicity and improve outcomes in patients with haematological malignancy and haemopoietic stem cell transplant recipients, 2021. Intern Med J. 2021;51 Suppl 7: 37–66.
消化器症状も少なく、嘔気2.4〜5.8%、嘔吐2.8〜5.1%、下痢2.1〜5.8%です。低K血症は0.4〜6.8%に留まっています。IRAEは0〜17%と報告によって幅がありますが、総じて1時間かけると少なくなります。
相互作用
添付文書ではシロリムスと併用注意と記載されています。アゾール系と比べると相互作用はとても少ないです。
CPFGはタクロリムスの濃度を下げることが知られていますが、MCFGはタクロリムス濃度への影響は乏しいです。
シクロスポリンはCPFGの濃度を上げることが知られていますが、シクロスポリンのMCFG濃度への影響は乏しいです。
| MCFG | CPFG | |
|---|---|---|
| ローディング投与 | なし | あり |
| 腎障害での減量 | なし | なし |
| 肝障害での減量 | なし | あり |
| 相互作用 | 少ない | CPFGはTac濃度を下げる CsAはCPFG濃度を上げる |
MCFGの投与量とエビデンス
50mg
MCFG 50mgは予防投与量です。
造血幹細胞移植患者882名の好中球減少時に、MCFG 50mgとFLCZ 400mgを比較した試験があり、MCFG 50mgのほうが真菌感染を防ぎました。この試験では抗真菌薬予防投与期間は、生着後5日以内あるいは移植後42日目まででした。
| MCFG | FLCZ | |
|---|---|---|
| 投与症例数 | 425名 | 457名 |
| 用量 | 50mg | 400mg |
| Primary Endpoint 侵襲性真菌感染症の 予防成功率 | ||
| 侵襲性カンジダ症 | 4例 | 2例 |
| 侵襲性アスペルギルス症 | 1例 | 7例 |
| ムーコル症 | 1例 | 0例 |
| フサリウム症 | 2例 | 1例 |
| Safety 肝障害 | 5.2% | 6.8% |
100〜150mg
MCFG 100〜150mgは治療投与量です。
1つの考え方として、カンジダをターゲットとする時に100mgを、アスペルギルスをターゲットとする時に150mgを用いるというものがありますが、MCFGの効果は用量依存性がある点に注意します。
HIV陽性患者における、内視鏡と培養で証明された食道カンジダ症に対して、MCFG 50mg、100mg、150mgを14〜21日間投与した用量反応試験では、内視鏡的治癒率はそれぞれ68.8%、77.4%、89.8%で用量依存性がありました。 MCFG 100〜150 mgによる内視鏡的治癒率(83.5%)は、FLCZ 200mgによる内視鏡的治癒率(86.7%)と同等でした。
| MCFG 50mg | MCFG 100mg | MCFG 150mg | FLCZ 200mg | |
|---|---|---|---|---|
| 内視鏡的治癒率 | 68.8% | 77.4% | 89.8% | 86.7% |
300mg
安全性について東大血液腫瘍内科から後方視的観察研究が報告されており、副作用は300mgと150mgで同等でした。具体的な副作用としては肝障害が多く、他に高血圧と下痢も多かったとのことです。
| 300mg | 150mg | |
|---|---|---|
| 症例数 | 26名 | 58名 |
| 副作用 | ||
| 肝障害 |
CPFGはシクロスポリンとの相互作用がありますが、MCFG300mgはシクロスポリンとの相互作用は問題ないと報告されています。Inoue Y, Saito T, Ogawa K, Nishio Y, Kosugi S, Suzuki Y, Kato M, Sakai T, Takahashi M, Miura I. Drug interactions between micafungin at high doses and cyclosporine A in febrile neutropenia patients after allogeneic hematopoietic stem cell transplantation. Int J Clin Pharmacol Ther. 2012 Nov;50(11):831-7.
まとめ
- MCFGはβ-(1,3)-Dグルカン合成を阻害し、カンジダに殺菌的に、アスペルギルスに静菌的に作用する。β-(1,6)-Dグルカンが主体のムーコル、フサリウム、トリコスポロン、クリプトコックス、α-Dグルカンが主体の酵母相の二相性真菌に効果が乏しい。
- 予防の例 MCFG 50mg + 生食100mL 1日1回30分でdiv
治療の例 MCFG 100〜150mg + 生食100mL 1日1回1時間でdiv - CNSへの移行性は不良。主な副作用は肝障害。肝障害・腎障害での減量なし。