2022年のBloodに中枢神経系原発悪性リンパ腫(PCNSL:Primary Central Nervous System Lymphoma)のReviewがありました。このReviewを中心に気になったところをまとめます。
- B症状はまれ
- 全身の評価:PET・骨髄検査・精巣エコー
- 神経の評価:MRI(脳と脊髄)・髄液検査・細隙灯顕微鏡検査
- 生検を急ぎ、神経系の回復を目指して、すぐにステロイドを導入する
- 予後予測モデルにMSKCCとIELSG
- InductionにHD-MTXを含める
- Consolidationは若年ならASCT
- 発症機序からBTK阻害薬に期待
- IMiDsも有望
- 治療後2年間は3か月毎のMRIでフォロー → 3〜5年目は半年毎 → 6年目から1年毎
診断
B症状はまれ
PCNSLは9割がDLBCLですが、全身性DLBCLとは違って、B症状はまれです。
では、どんな症状がヒントになるか?という点ですが、
- 50〜70%で、何らかの神経学的欠損があります。
- 40〜50%で、週から月単位で進行する、認知や行動の非特異的な変化だけのこともあり、「なんとなく変」でも注意を要します。
- 33%で、頭痛・嘔気・嘔吐があります。

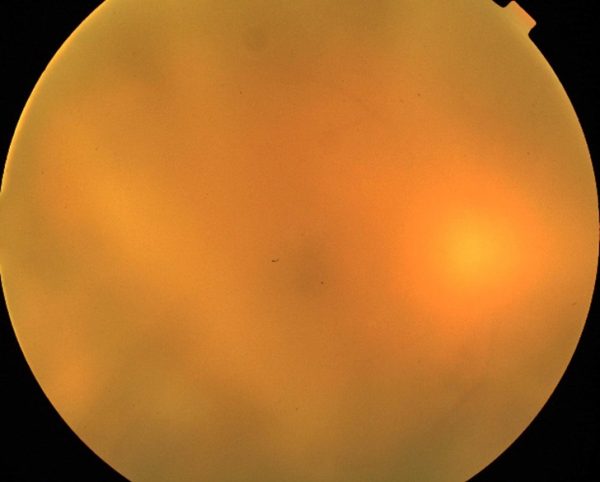
なお、眼内悪性リンパ腫では、眼がかすんだり、視力が下がったりしますが、視覚異常がないことも多く、ぶどう膜炎とも紛らわしいです。
全身の評価:PET・骨髄検査・精巣エコー
Visual Abstractが提供されていて、全体像が分かりやすいです。ただし後述の注意点があります。
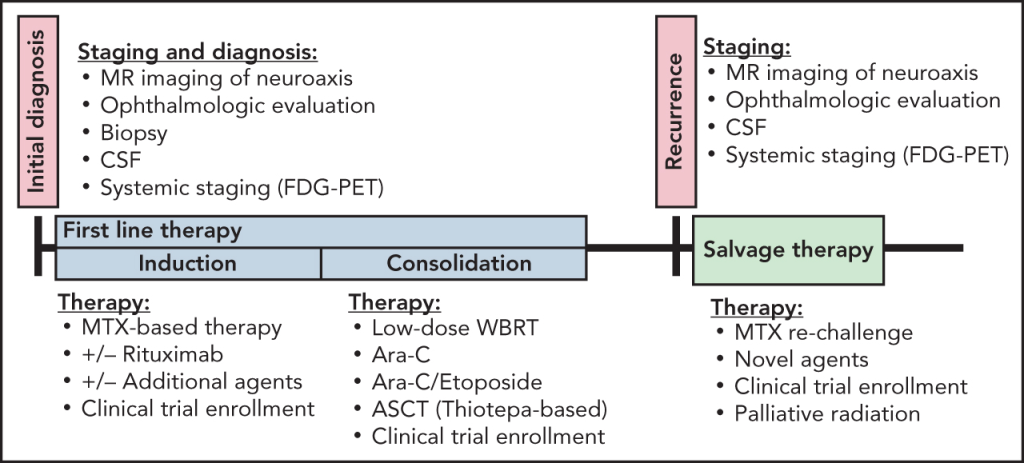
上のVisual Abstractでは、骨髄検査と精巣エコー(男性)に言及がないですが、必須です。精巣原発悪性リンパ腫は中枢神経系に入り込みやすいことを十分に念頭に置く必要があります。

PCNSLを疑われた症例のうち、4〜7%で、CNS外の病変が見つかっています。
すなわち、リンパ腫の脳病変があった時には、PCNSLなのか、SCNSLなのか鑑別を要します。「よく調べたらSCNSL等でした」という症例のまとめも報告されています。

神経の評価:MRI(脳と脊髄)・髄液検査・細隙灯顕微鏡検査
MRIは脳だけでなく、脊髄も撮ります。
脳MRIでは、脳室周囲に多発することが特徴です。深い部分に多発するため、手術で切除することは難しいです。他の脳腫瘍と比較すると、脳浮腫は少ないようです。
髄液検査では、一般(蛋白や糖を含む)・細胞診に加えて、FCM、遺伝子再構成も提出したいところです。
眼科で、細隙灯顕微鏡検査(Slit Lamp Examination)を行っていただきます。
生検を急ぎ、神経系の回復を目指して、すぐにステロイドを導入する
神経系の回復を目指して、できるだけ早期にステロイドを開始します。スピードが重要です。
ただし、生検前にはステロイドは極力入れたくないです。
それでも、どうしてもステロイドを入れざるを得ない時もあります。下記のように言及されていました。
If it is necessary to start steroids, a brain biopsy should be performed within 24 to 48 hours of the first dose to optimize the diagnostic yield.
Schaff LR, Grommes C. Primary central nervous system lymphoma. Blood. 2022;140: 971–979.
なお、脳生検後に、ステロイド開始にあたって、傷の回復を待つべきではありません。
予後予測モデルにMSKCCとIELSG
PCNSLの予後予測モデルには、MSKCCのスコアと、IELSGのスコアの2つがあります。
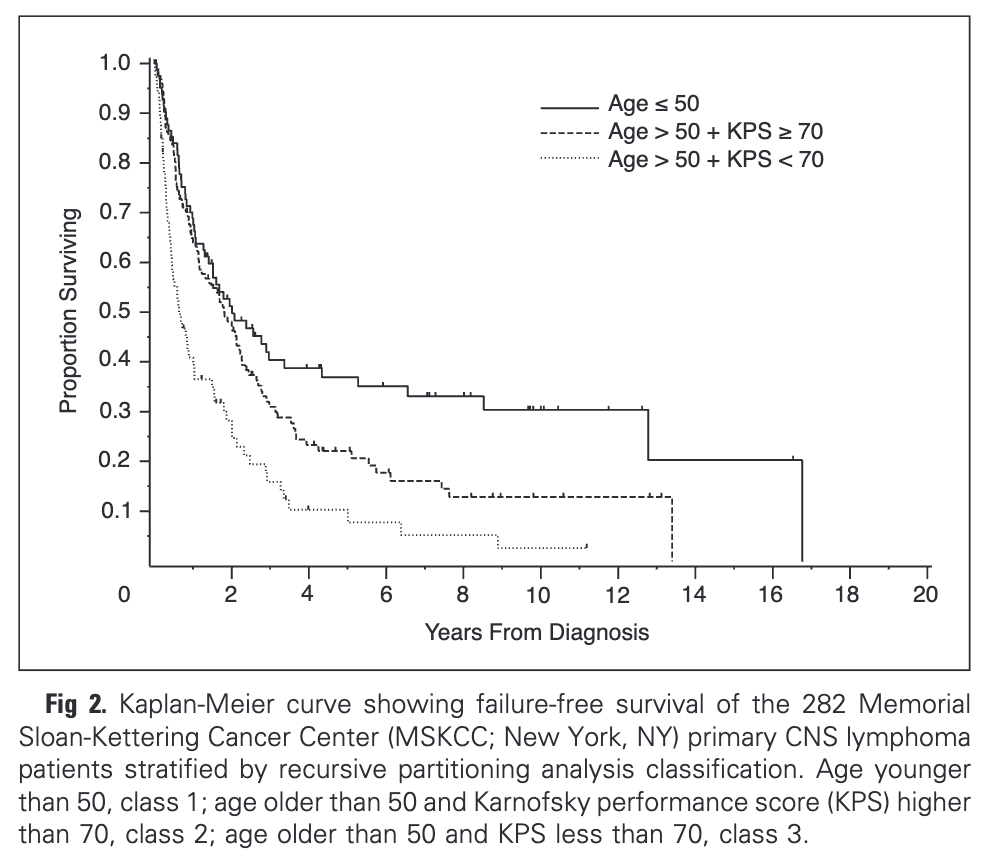
まず、MSKCC(Memorial Sloan Kettering Cancer Center)のスコアです。
| 分類 | 基準 | OS | FFS |
|---|---|---|---|
| class 1 | 50歳以下 | 8.5年 | 2.0年 |
| class 2 | 51歳以上 かつ KPS 70%以上 | 3.2年 | 1.8年 |
| class 3 | 51歳以上 かつ KPS 60%以下 | 1.1年 | 0.8年 |
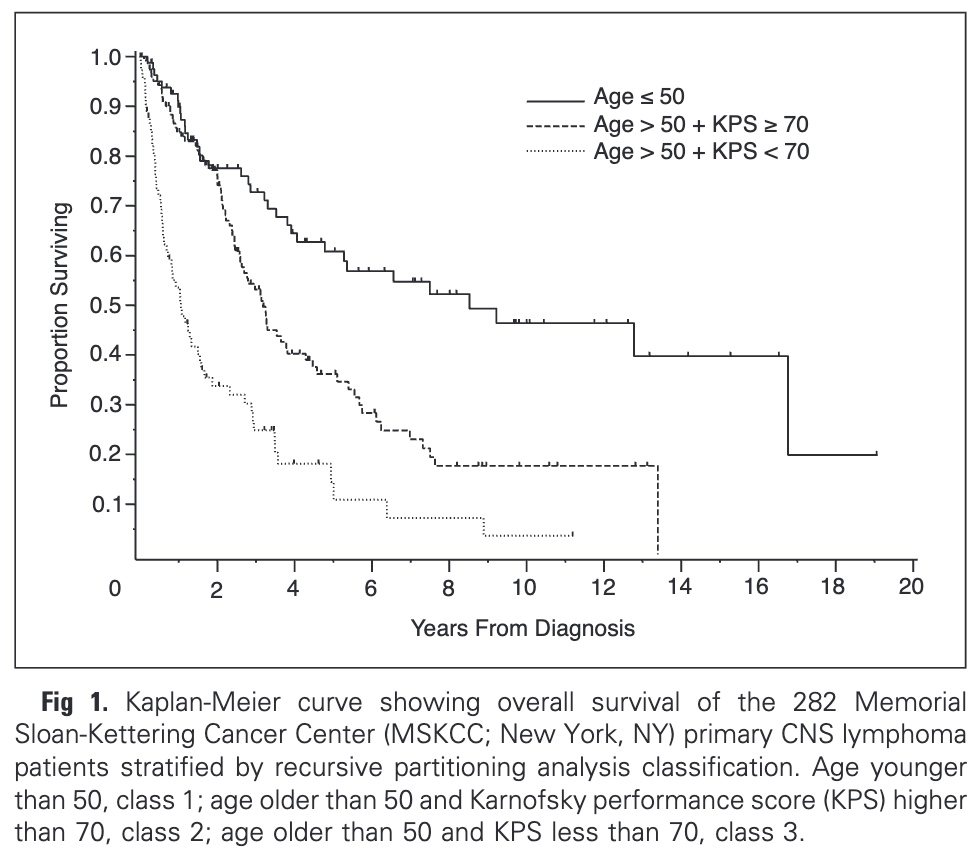
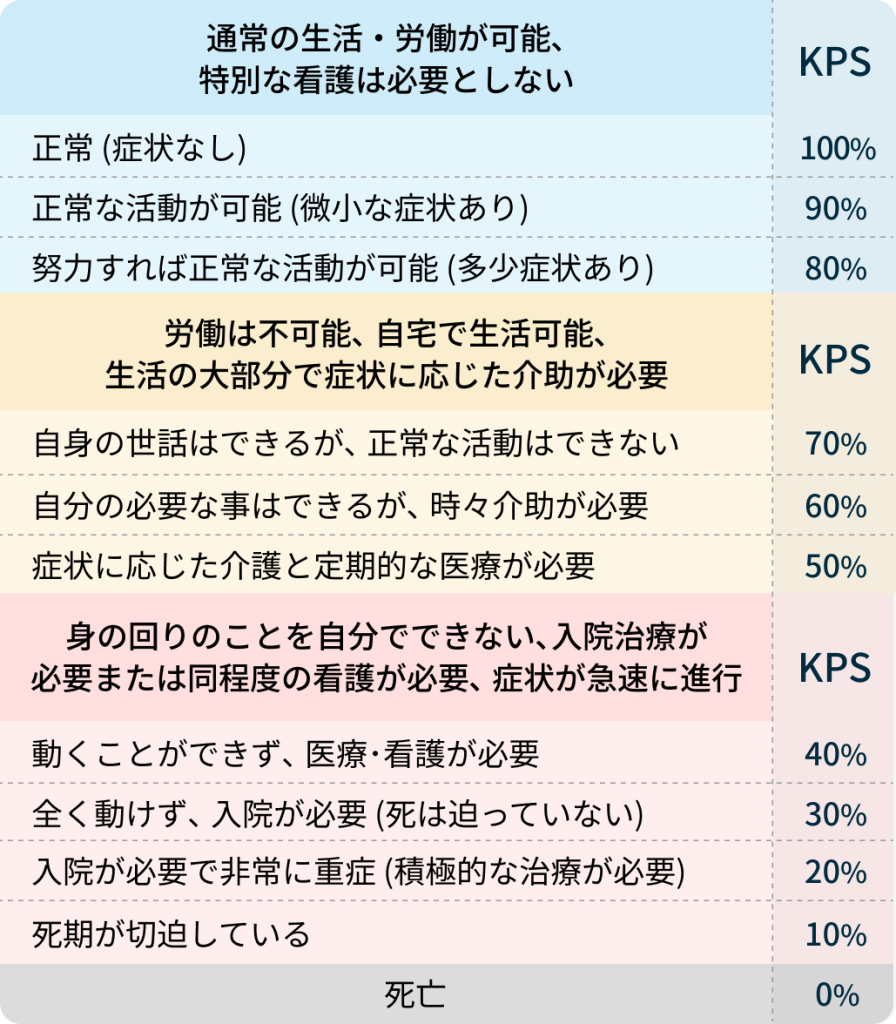
なお、KPSは下記です。
続いて、IELSG(International Extranodal Lymphoma Study Group)のスコアです。
| 項目 | あり | なし |
|---|---|---|
| 61歳以上 | 1点 | 0点 |
| PS 2以上 | 1点 | 0点 |
| LDH 上昇 | 1点 | 0点 |
| 髄液蛋白 上昇 | 1点 | 0点 |
| 脳深部への浸潤 (脳室周囲・基底核・脳幹・小脳) | 1点 | 0点 |
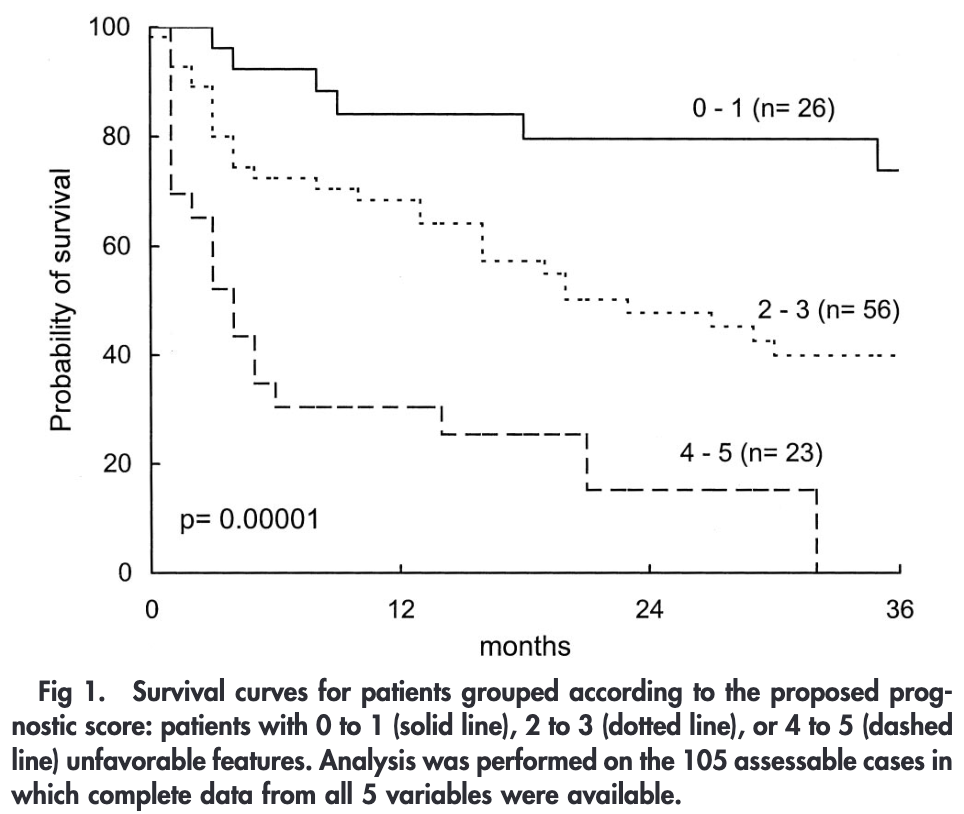
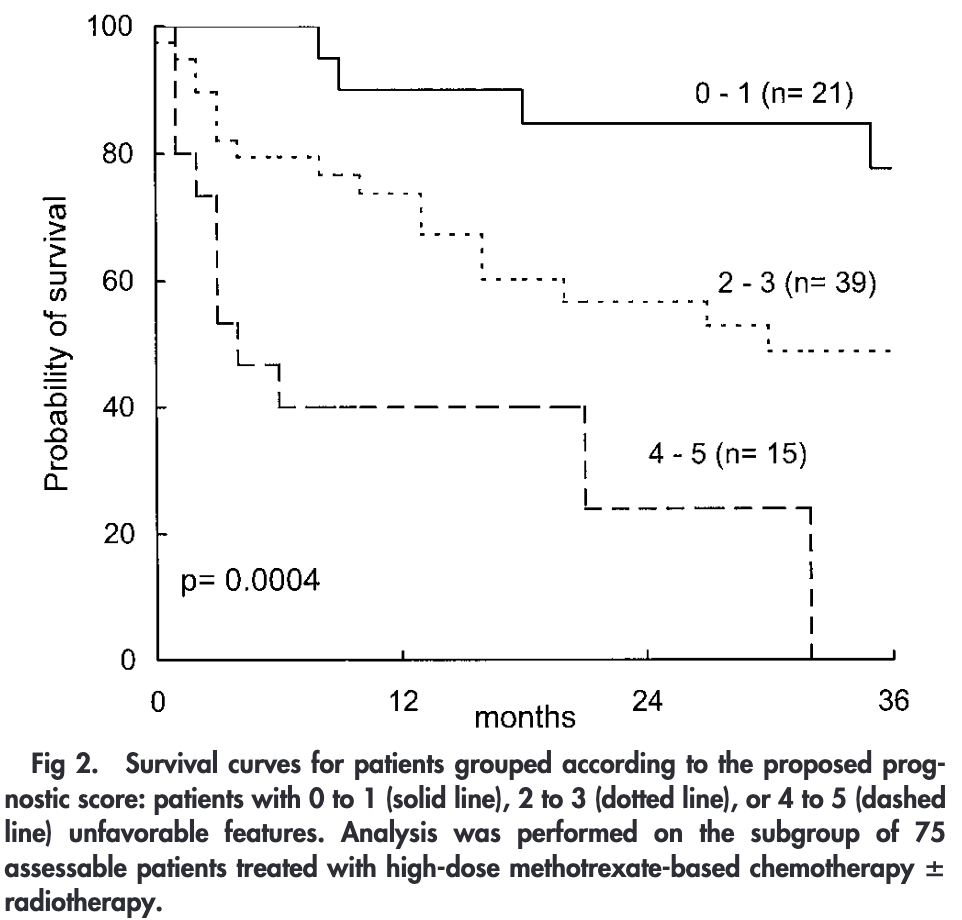
| IELSGスコア | 2y-OS | 2y-OS (HD-MTX治療群) |
|---|---|---|
| 0〜1点 | 80% | 85% |
| 2〜3点 | 48% | 57% |
| 4〜5点 | 15% | 24% |
治療
InductionにHD-MTXを含める
MTX>1.5 g/m2でBBBを突破できます。
日本では、R-MPV療法(リツキシマブ・HD-MTX・プロカルバジン・ビンクリスチン)が行われています。
HD-MTXを核とした1st lineのデータを下記に引用します。
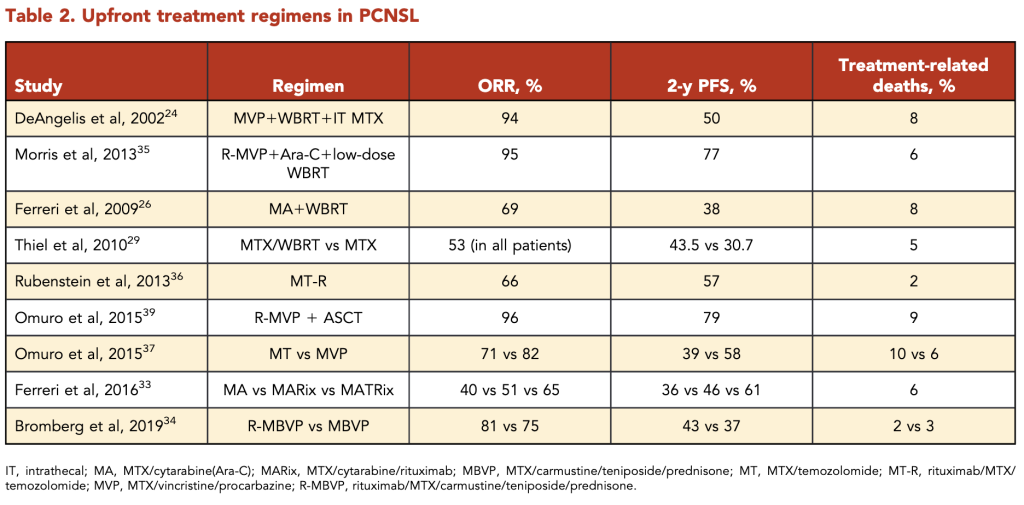
再発した時にも、1st lineのHD-MTXで長期的に寛解維持できたならば、HD-MTXの再投与も選択肢になります。
全脳照射(WBRT)は、寛解には入りやすいですが、効果は長続きせず、また認知機能低下も懸念され、近年1st lineでは避けられるようになりつつあります。
Consolidationは若年ならASCT
チオテパ(商品名:リサイオ)を移植前処置に用いた時の成績がよいです。
発症機序からBTK阻害薬に期待
そもそも、PCNSLは大部分がDLBCLで、さらにABC typeとされています。
MYD88やCD79Bの変異によって、BCR pathwayの異常が生じており、そこにアプローチするBTK阻害薬に期待がかかります。
すでに日本ではチラブルチニブ(商品名:べレキシブル)が保険適用となっています。
IMiDsも有望
レナリドミド(商品名:レブラミド)、ポマリドミド(商品名:ポマリスト)といったIMiDsにも有望なデータが出てきているようです。
特にレナリドミドは、リツキシマブと併用したデータもあるようで、まるで濾胞性リンパ腫へのR2療法のように、相乗効果があるのかもしれません。下記にサルベージのデータを引用します。
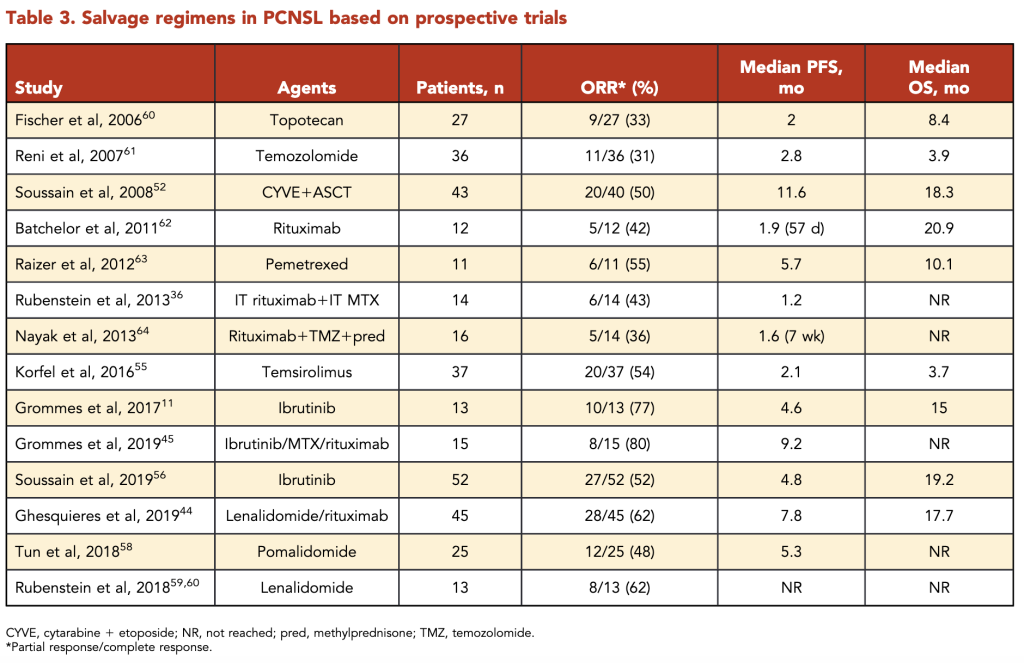
治療後2年間は3か月毎のMRIでフォロー → 3〜5年目は半年毎 → 6年目から1年毎
NCCNの推奨するフォロー方法とのことです。
まとめ
怒涛の復習です。
- B症状はまれ
- 全身の評価:PET・骨髄検査・精巣エコー
- 神経の評価:MRI(脳と脊髄)・髄液検査・細隙灯顕微鏡検査
- 生検を急ぎ、神経系の回復を目指して、すぐにステロイドを導入する
- 予後予測モデルにMSKCCとIELSG
- InductionにHD-MTXを含める
- Consolidationは若年ならASCT
- 発症機序からBTK阻害薬に期待
- IMiDsも有望
- 治療後2年間は3か月毎のMRIでフォロー → 3〜5年目は半年毎 → 6年目から1年毎
参考資料
今回の記事ではBlood 2022のPCNSLのReviewを主に参照しました。Blood 2023のHow I treatシリーズでSCNSLがまとめられており、そちらも気になります。
Blood 2022のReviewと同じグループがJCO 2017でもReviewを書いており、引用数が300を超えています。
日本脳腫瘍学会から「脳腫瘍診療ガイドライン 成人脳腫瘍編 2019年度版(改訂版)」が発表されており、その中に「中枢神経系悪性リンパ腫ガイドライン」が含まれています。ただし、自家移植を推奨しないと記載されていますが、2023年現在は自家移植のエビデンスが充実し、実臨床において、若年者であれば自家移植を行うことが多いです。